Trotz der großen und zunehmenden Bedeutung, die Dengue-Fieber (DF) für die Gesundheit der Menschen weltweit hat, gibt es nur wenig überzeugende Impfstoffe, die bisher zugelassen sind. Als ein Hauptproblem der jahrzehntelangen Impfstoffentwicklung stellt sich immer wieder das so genannte antibody dependent enhancement (ADE) heraus.
Antikörper gegen die vier existierenden Dengue-Serotypen (DENV 1-4) sind zwar kreuzreaktiv, aber nicht anhaltend kreuzprotektiv:
Nach der Infektion mit einem der Serotypen besteht für einen begrenzten Zeitraum von etwa 2 Jahren ein Schutz auch vor Ansteckung mit den anderen DENV (Halstaed 2022), dieser lässt dann jedoch nach und die weiter vorhandenen, aber nicht mehr schützenden Antikörper erhöhen im Fall einer späteren Zweitinfektion mit einem anderen Serotypen das Risiko schwerer Verläufe: sie bilden dann mit den DENV Immunkomplexe, die die Vermehrung der Viren und die Bildung eines viralen Toxins (NS1) letztendlich massiv steigern und zu den schweren Verlaufsformen des Dengue-Fiebers (DHF, DSS) führen (s. hier).
Dieses Phänomen hat in der Entwicklung der Impstoffe immer wieder zu einer Erhöhung des Risikos schwerer Verläufe auch durch die Impf-Antikörper geführt und ist bis heute weder vollständig verstanden noch gelöst.
Dengvaxia™ war der erste zugelassene Dengue-Impfstoff, hergestellt von Sanofi Pasteur (SP). Er beruht auf dem Gelbfieber-Impfvirus von SP, bei dem gentechnisch entscheidende Proteine aller 4 Serotypen des DNV eingefügt wurden. Als Lebendimpfstoff enthält Dengvaxia™ kein Aluminium oder andere Wirkverstärker und soll weder schwangeren noch stillenden Frauen oder Menschen mit geschwächtem Immunsystem verabreicht werden.
Die in den Zulassungsstudien durch drei Impfdosen im Abstand von jeweils 6 Monaten entstehende Impfstoff-Wirksamkeit hing von verschiedenen Faktoren ab:
-
sie war nicht für alle 4 DENV-Typen gleich, mit niedriger Wirksamkeit gegen v.a. DENV-1 und-2 - Fachleute sprechen von einem "funktionell monovalenten Impfstoff gegen DENV 4" (Silva 2023)
-
sie war signifikant niedriger bei seronegativen Geimpften, also Menschen, die vor der Impfung noch mit keinem der DENV-Typen infiziert waren
-
sie war nicht nur auffallend niedrig für jüngere Kinder, Kinder unter 9 Jahren hatten nach der Impfung sogar ein signifikant höheres Risiko, wegen eines DF im Krankenhaus behandelt werden zu müssen (Silva 2023), bei Kindern unter 5 Jahren war dies im Vergleich zur Kontrollgruppe fast fünffach erhöht. Auch bei den 9 - 16-Jährigen waren die Rate schwerer Verläufe bei den geimpften seronegativen Kindern und Jugendlichen im Vergleich zu Ungeimpften erhöht, aufgrund der insgesamt geringen Fallzahlen war dies aber nicht statistisch signifikant (Halstead 2023). Dies wird als klarer Hinweis auf ein ADE gewertet: vor allem jüngere, meist seronegative Kinder werden durch die DF-Impfung sensibilisiert und haben bei einer späteren DENV-Wildvirus-Infektion durch das ADE ein deutlich erhöhtes Risiko für schwere Verläufe als ungeimpfte Kinder (Halstead 2017). Die Frage, warum hier vor allem Kinder (stärker als andere seronegative Geimpfte) betroffen sind, ist unverstanden und ungeklärt (Halstead 2023).
Diese Daten führten dazu, dass Indonesien die Zulassung für Dengvaxia dauerhaft widerrief (DÄ 2023) und die WHO die Zulassung von Dengvaxia™ ausdrücklich nur für Erwachsene und Kinder älter als 9 Jahre und in Regionen empfiehlt, in denen die "Durchseuchung" mit DENV bei mindestens 70% liegt, also die meisten Geimpften schon vor der Impfung seropositiv für DENV sind (Halstead 2023). Dem letzten Punkt trägt die EMA bei ihrer Zulassung Rechnung, indem sie den Nachweis einer vor der Impfung abgelaufenen DF-Erkrankung (klinisch oder serologisch) zur Bedingung für die Impfung macht, sie setzt die Zulassungsgrenze mit 6 Jahren allerdings deutlich niedriger als von der WHO empfohlen (EMA 2022a).
Der industrieunabhängige "Arzneimittelbrief" (AMB 2023) zieht das Fazit: "Kinder, die bisher keine Dengue-Fieber-Infektion durchgemacht haben – also seronegativ sind – sollten nach den Ergebnissen der hier besprochenen Studie [Sridhar 2018] nicht gegen Dengue-Fieber geimpft werden, da geimpfte Kinder bei einer nachfolgenden Infektion mit Dengue-Viren ein erhöhtes Risiko für einen schweren Verlauf haben. Diese Empfehlung dehnen wir auch auf Erwachsene aus." Der AMB betont ausdrücklich, dass er diese deutlich zurückhaltende Einschätzung unabhängig von zukünftig zu erwartenden RKI/STIKO-Empfehlungen ausspricht und beibehalten wird.
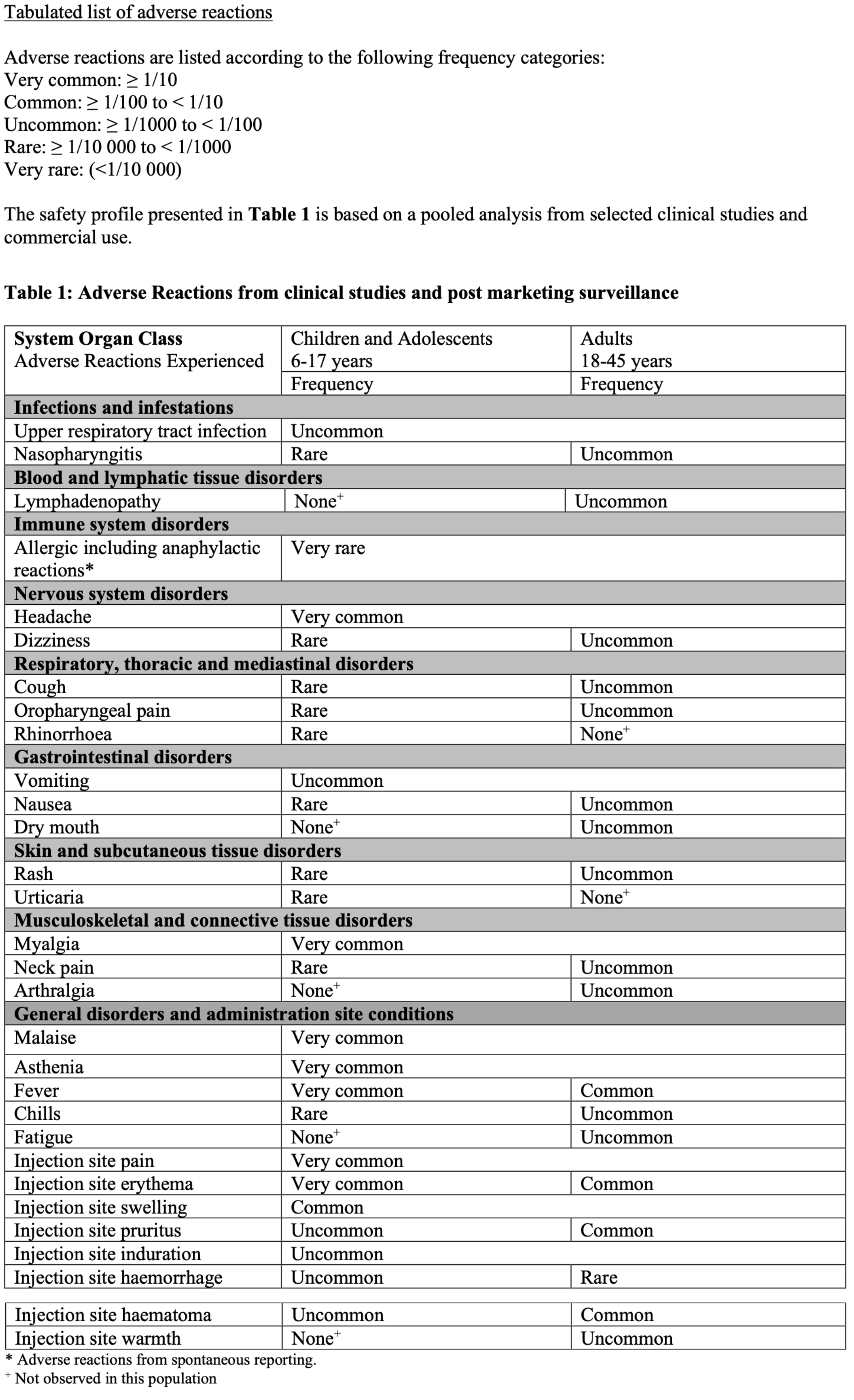
Im Vergleich zu diesen grundsätzlichen Problemen der Impfung gerade bei Kindern treten die anderen beobachteten Nebenwirkungen der Impfung deutlich in den Hintergrund:
(EMA 2022a)
Auch Qdenga™ der Firma Takeda ist ein genetisch hergestellter Lebendimpfstoff, der allerdings als "Trägervirus" ein DENV verwendet (Serotyp 2), in das Antigene der anderen DENV-Serotypen eingebaut wurden.
Verabreicht werden hier nur zwei Impfdosen im Abstand von 3 Monaten.
In den Zulassungsstudien mit insgesamt 27 Monaten Nachbeobachtungszeit zeigte sich
-
eine deutlich unterschiedliche Wirksamkeit gegen die einzelnen Serotypen mit der größten Effektivität gegen DENV-2 (das Trägervirus) und der schlechtesten gegen DENV-3; gegen DENV-4 konnte aufgrund der geringen Fallzahlen keine sichere Effektivität bestimmt werden.
-
dass auch Qdenga™ bei seronegativen Geimpften eine geringere Impfstoff-Effektivität aufwies als bei bereits vor der Impfung seropositiven (67% vs. 74,8% kumulativ; Silva 2023)
-
eine Impfstoff-Effektivität von 80,2% 12 Monate nach der zweiten Impfdosis, die allerdings im zweiten Jahr nach der Impfung deutlich nachließ (56,2%), vor allem bei kleinen Kindern (bei 4/5-Jährigen auf 24,5%, Vertrauensbereich -34,2 - 57,5%), 60,6% bei den 6 - 11-Jährigen und 71,2% bei den 12 - 16-Jährigen mit jeweils weniger absurden Vertrauensbereichen. Im zweiten Jahr nach der Impfung stieg die Zahl der wegen DF hospitalisierten geimpften Kindern bei geringen Gesamtzahlen deutlich an, ein Warnsignal für ein mögliches ADE (Halstead 2023).
- eine Virämie des Impfvirus bei bis zu 49% der ungeimpften Studienteilnehmer (16% der geimpften), die mit grippalen Symptomen des DF einherging und grundsätzlich das Risiko der Weiterverbreitung des Impfvirus durch Stiche geeigneter Vektoren in dieser Zeit in sich birgt (EMA 2022b).
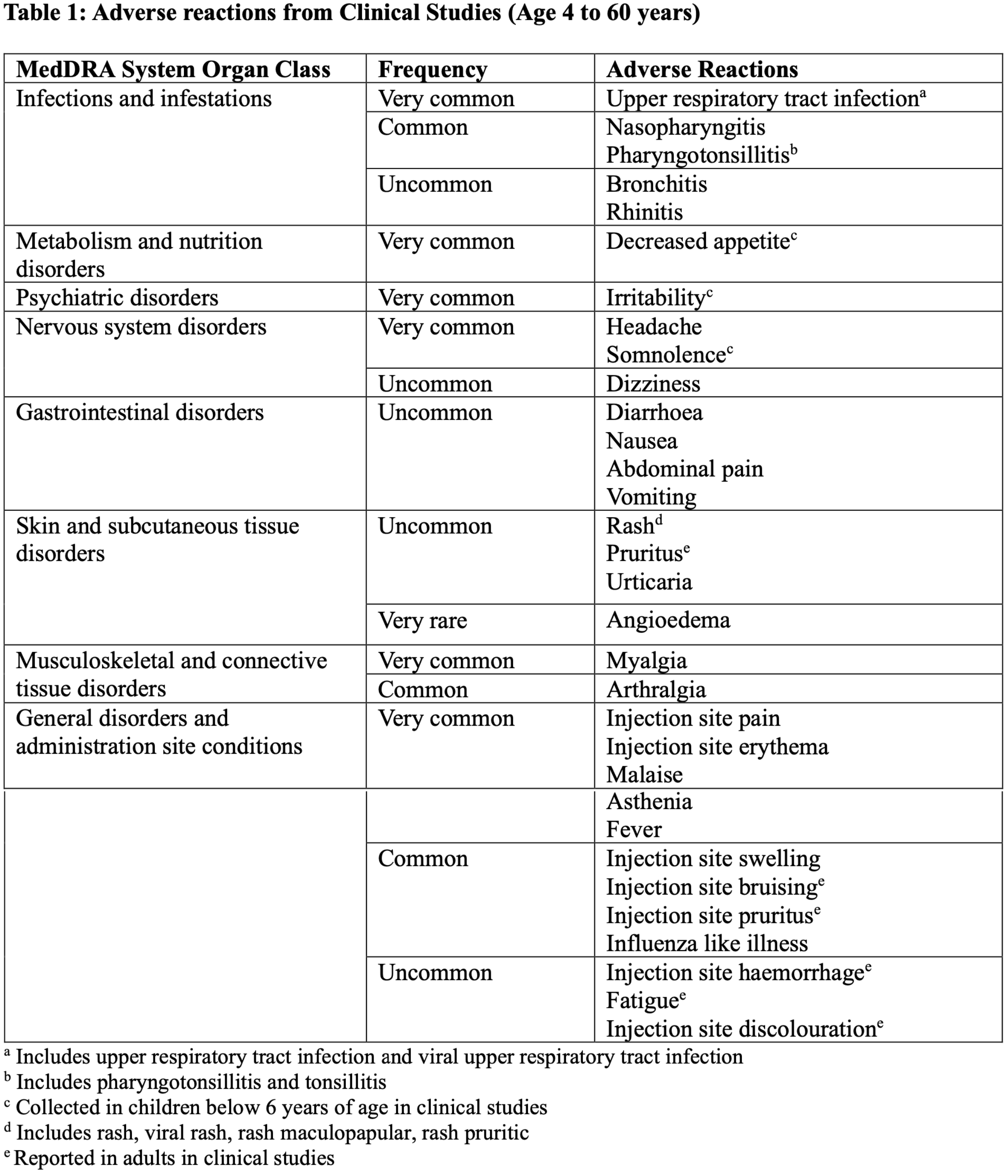
Andere UAW wie von der EMA dokumentiert:
(EMA 2022b)
AMB. 2023. 57, 80DB01
DÄ. 2023. https://www.aerzteblatt.de/nachrichten/101203/Philippinen-ziehen-Lizenz-fuer-Dengue-Impfung-nach-Todesfaellen-zurueck. Abruf 25.10.2023
EMA. 2022a. Dengvaxia EPAR. Abruf 18.10.2023
EMA. 2022b. Qdenga EPAR. Abruf 18.10.2023
Halstead SB. 2022. Denguevirus-Vaccines. In Plotkin's Vaccines, 8th ed., 2022.
Halstead SB. 2017. https://doi.org/10.1016/j.vaccine.2017.09.089. Abruf 18.10.2023
Silva P. 2023. Journal of General Virology 2023;104:001831 DOI 10.1099/jgv.0.001831
Sridhar S. 2018 N. Engl. J. Med. 379, 327.