Spätestens seit dem Inkraft-Treten des so genannten Masernschutzgesetzes ist das Thema der Antikörper-Bestimmung auch jenseits medizinischer Fachkreise ein Thema - schreibt das Gesetz doch "nur" den Nachweis einer Immunität (und nicht etwa: eine bestimmte Anzahl von Impfungen) vor.
Die moderne Masernimpfung ist immer eine Lebendimpfung: verimpft werden also lebende, vermehrungsfähige, aber durch verschiedene Laborverfahren abgeschwächte Masernviren. Obwohl viele der heute international verwendeten Masern-Impfvirus-Stämme letztendlich vom so genannten Edmonston-Impfvirus abstammen, haben sich in verschiedenen Regionen der Welt unterschiedliche Nachfahren dieses Urgroßvaters der Masern-Impfviren durchgesetzt, die sich vor allem in den Methoden der Anzucht und der Abschwächung unterscheiden. In der westlichen Hemisphäre (also auch in Europa) wird überwiegend der so genannte Schwarz-Stamm (SW) eingesetzt, wogegen z.B. in Indien (und auch in Kroatien) Impfviren des Stammes Edmonston-Zagreb (EZ) Verwendung finden (Strebel 2017).
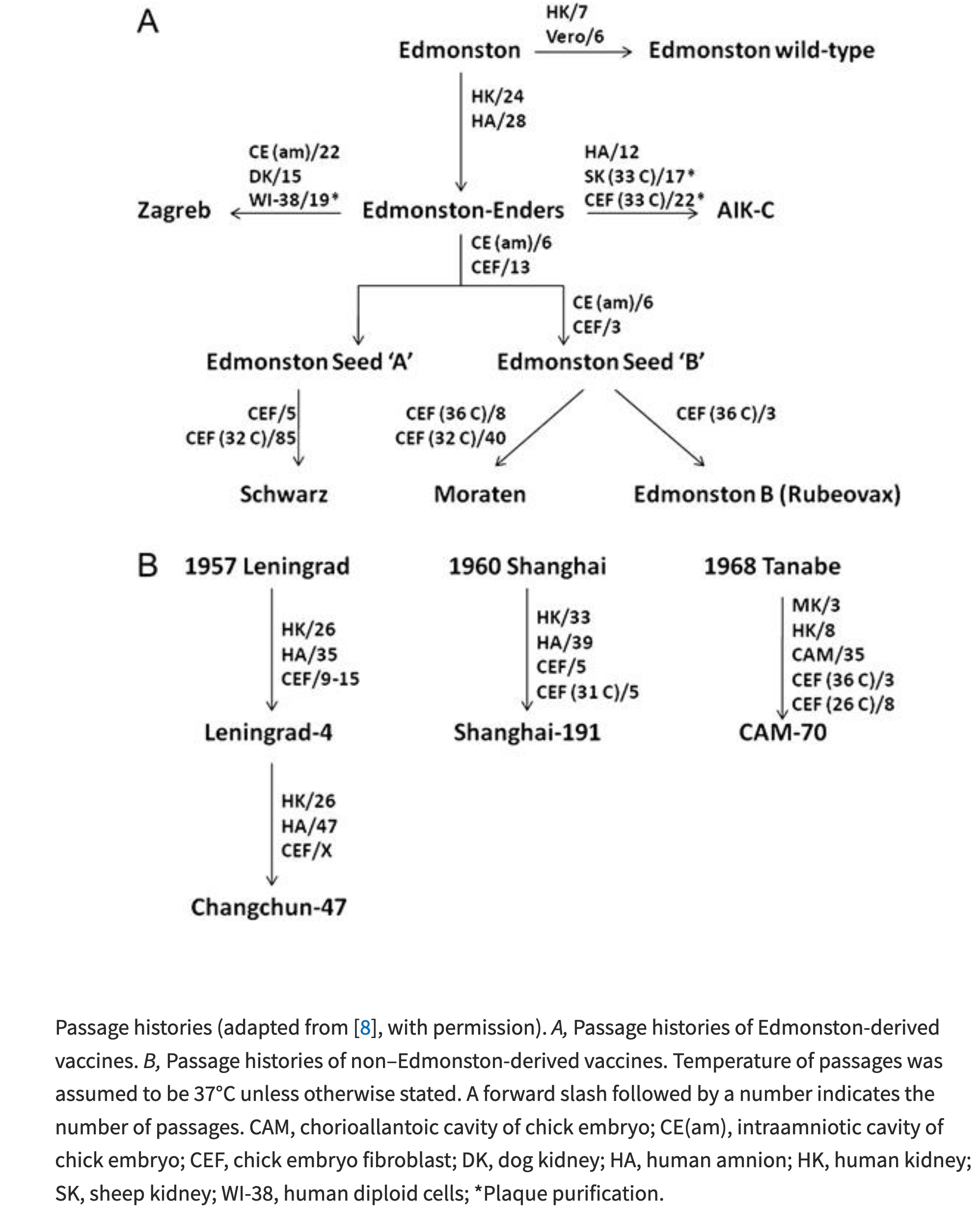
Hier ein Stammbaum der verwendeten Impfviren (Bankampf 2011)
[[8]: Rota JS. 1994 Virus Res. vol. 31]
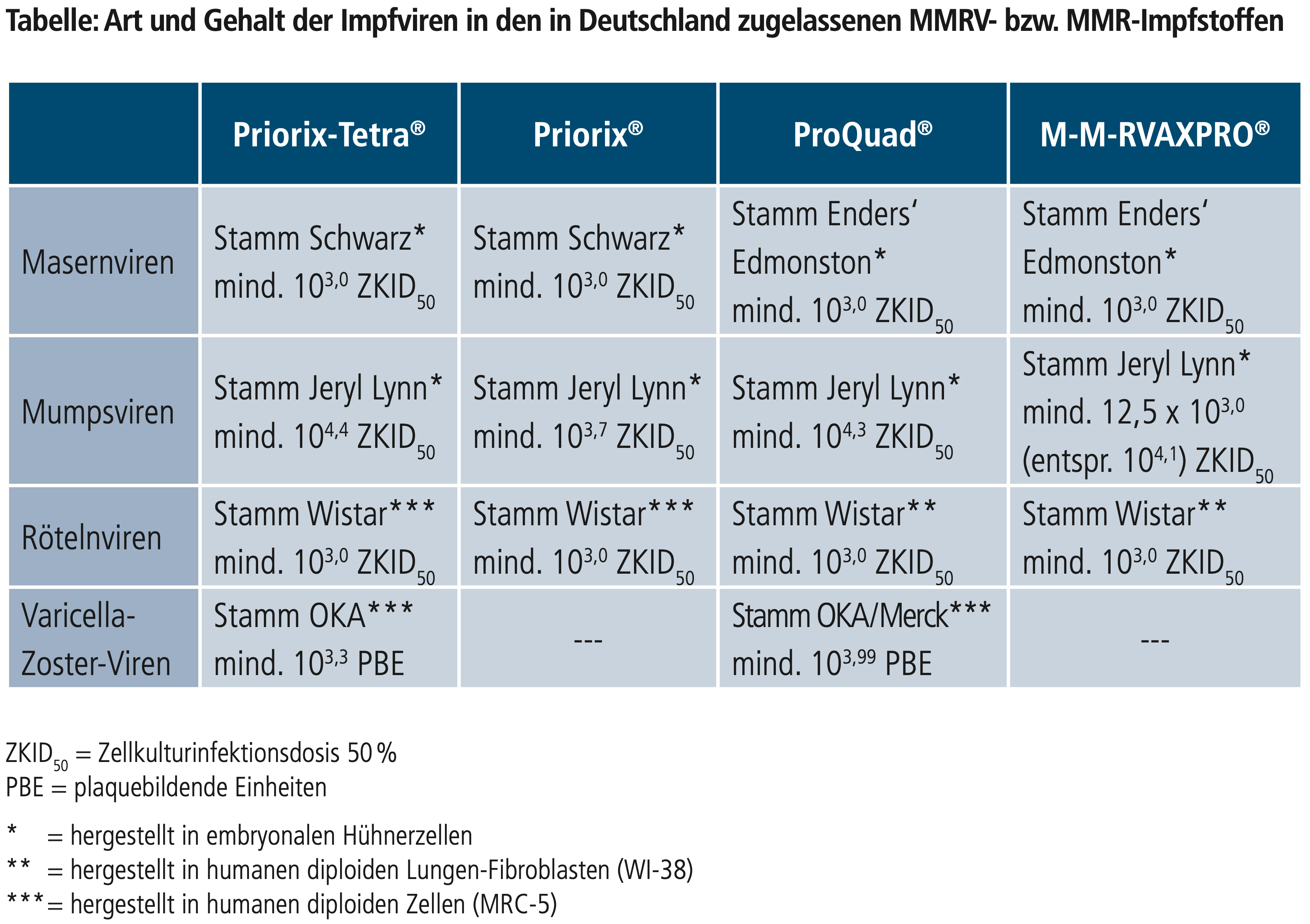
Hier eine Übersicht der in Deutschland verwendeten Masern-haltigen Impfstoffe (PEI 2011)
Obgleich als grundsätzlich vergleichbar wirksam angesehen, scheinen sich die Vor- und Nachteile der Impfstämme zu unterscheiden:
-
so erzeugt der EZ auch schon bei sehr früher Erstimpfung vor dem ersten Geburtstag (und der damit verbundenen möglichen Gegenwart mütterlicher Leih-Antikörper im Serum) schon eine Serokonversion bei den meisten Geimpften. Dadurch wird dieser Impfstoff oft verwendet, wenn eine sehr frühe Erstimpfung notwendig ist und/oder aufgrund einer hohen Prävalenz der Masernerkrankung häufig noch ein länger anhaltender Nestschutz anzunehmen ist. Die mit EZ erreichten Antikörper-Titer sind jedoch in der Regel niedriger, als die mit SW erzielten.
-
SW erzeugt höhere Antikörper-Spiegel, vor allem in Abwesenheit mütterlicher Leih-Titer und wird daher in Regionen verwendet, in denen die Erstimpfung nach dem ersten Geburtstag erfolgt und die Masern-Erkrankungshäufigkeit eher niedrig ist (Martins 2013, Bennett 1999).
- Zusammengefasst erzeugt EZ also häufiger eine Serokonversion nach der Impfung (also das messbare Entstehen einer Immunität), führt dabei aber zu insgesamt niedrigeren Antikörper-Titern (Hussey 1996).
Auch bei der Bestimmung der Masern-Antikörper (egal ob nach Impfung oder nach durchgemachter Erkrankung) lassen sich mindestens zwei relevante Testverfahren unterscheiden:
-
der so genannte Plaque Reduction Neutralisation Test (PRNT)
-
und der so genannten Enzyme-Linked Immunosorbent Assay (ELISA).
Der PRNT gilt international als "Goldstandard", misst er doch unmittelbar die für die humorale Immunität (s. hier) letztendlich entscheidenden neutralisierenden Antikörper (Korrelat der humoralen Immunität). Er ist aber technisch, zeitlich und apparativ sehr aufwändig und arbeitet darüber hinaus mit lebenden Masernviren, wodurch eine Standardisierung zwischen verschiedenen Labors schwierig ist (Cohen 2008).
Der ELISA ist im Vergleich zum PRNT schneller, kostengünstiger, automatisierbar und leichter zu standardisieren, weshalb er sich in den letzten Jahren in den meisten europäischen Labors als Standardmethode der Antikörperbestimmung (nicht nur bei Masern) durchgesetzt hat. Er ist aber bekanntermaßen weniger sensitiv, das heißt: er entdeckt eine bestehende Immunität weniger zuverlässig als der PRNT, weil die gemessenen IgG-Antikörper nicht unmittelbar mit der tatsächlichen Immunität korrelieren, sie sind "nur" ein so genanntes Surrogat der Immunität (s. hier). Mit anderen Worten: zeigt der ELISA nach einer Masernimpfung keinen sicheren Schutz, lässt sich bei einem nicht kleinen Anteil der Geimpften mit dem PNRT doch noch eine Immunität nachweisen (dieses Phänomen beschreibt man mit dem Begriff des negativ prädiktiven Wertes NPW: bei wieviel im ELISA test-negativen Menschen lassen sich auch im PRNT keine Antikörper finden). Quantitative Vergleiche von ELISA und PNRT bei Masern-Antikörpertitern fanden teilweise NPWs von unter 50%, d.h. mehr als die Hälfte der im ELISA vermeintlich "Nicht-Immunen" erweist sich im PNRT als dennoch immun (Cohen 2008, Mancuso 2008).
Bis April 2018 war in der EU der Masern-Einzelimpfstoff Rouvax® der Firma Sanofi zugelassen (in Deutschland unter dem Namen Masern Mérieux® auf dem Markt), dessen Produktion im Sommer 2017 eingestellt wurde; letzte Chargen auf dem Markt verfielen mit Datum April 2018. Die Antikörper-Bestimmung nach diesem Impfstoff unterscheidet sich nicht grundsätzlich von der nach MMR-Impfstoffen.
Im November 2023 wurde in der Schweiz der Vertrieb von Measles Vaccine live® des Serum Institute of India (der den in Indien üblichen Impf-Stamm Edmonston-Zagreb verwendete) eingestellt, letzte verfügbare Chargen verfielen Ende März 2024. Damit ist in Europa derzeit (2024) kein Masern-Einzelimpfstoff verfügbar.
Die (begrenzte) Erfahrung mit Measles Vaccine live® bestätigt die oben ausgeführten Fakten zur Besonderheit der Antikörper-Bestimmung: die auf den in Europa üblichen Schwarz-Stamm kalibrierten, flächendeckend in den europäischen Labors verwendeten ELISA-Verfahren finden nach Impfung mit diesem Impfstoff häufig keine als sicher angesehenen Antikörper-Titer. Diese seien - so der Hersteller in persönlicher Kommunikation - mit dem PRNT jedoch zuverlässig nachweisbar: In einer mit diesem Impfstoff durchgeführten indischen Studie aus dem Jahr 2015 zeigte sich, dass die allermeisten positiven Ergebnisse im ELISA-Test sich im PRNT bestätigen ließen (96%, so genannter positiv prädiktiver Wert PPW), der so genannte negativ prädiktive Wert (NPW) des ELISA verglichen mit dem PRNT aber bei nur 69% lag, d.h. 31% der Proben, die im ELISA als negativ ausfielen, also keine Schutzwirkung annehmen ließen, zeigten in der Kontrolle mit dem PRNT dann doch eine Serokonversion, also Impfschutz (Low 2015). Es bleibt die technische Hürde, dass z.B. in Süddeutschland nur ein einziges größeres Labor (Labor Enders, Stuttgar) einen PRNT bei Masern überhaupt anbietet (zum etwa doppelten Preis des üblichen ELISA, s.o.). Die eigentlich sinnvolle Strategie, nach einer Masernimpfung ab dem zweiten Lebensjahr die fast immer entstehende Immunität durch eine Blutentnahme nachweisen zu lassen, gestaltet sich hier schwierig.
Bankamp B. 2011. Journal of Infectious Diseases, Volume 204, Issue suppl_1, S533–S548, https://doi.org/10.1093/infdis/jir097
Bennett JV. 1999. Pediatrics. 104(5):1123–1123
Cohen BJ. 2008. Vaccine. 26(50):6392–97
Hussey GD. 1996. Journal of Infectious Diseases. 173(6):1320–26
Low N. 2015. N Engl J Med. 372(16):1519–29
Mancuso JD. 2008. Vaccine. 26(38):4877–78
Martins C. 2013. Vaccine. 31(48):5766–71
PEI. 2011. Bulletin zur Arzneimittelsicherheit, Ausgabe 2.
Strebel PM. Measles Vaccines in Plotkin S. Plotkin's Vaccines 7th ed. Philadelphia 2017